|
办理环节
|
责任事项
|
承办科室
|
|
立案
|
1.立案责任:对检查中发现、接到群众举报投诉或经有关部门移送的未按规定实施质量管理规范等违法案件予以审查,决定是否立案。
|
稽查一大队
|
|
调查
|
2.调查责任:对立案的案件,案件承办人员及时、全面、客观、公正地调查收集与案件有关的证据,查明事实,必要时可进行现场检查;证据可能灭失或以后难以取得的,先行登记保存;与当事人有直接利害关系的应当回避;执法人员不得少于两人;调查取证时应出示执法证件;允许当事人辩解陈述。
|
稽查一大队
|
|
审查
|
3.审查责任:行政执法机关法制机构对案件违法事实、证据、调查取证程序、法律适用、处罚种类和幅度、当事人陈述和申辩理由等方面进行复核;行政机关负责人依法审查并作出处理意见,情节复杂或较重的行政处罚,由行政机关负责人集体研究。
|
行政事项服务科(政策法规科),稽查一大队
|
|
告知
|
4.告知责任:在做出行政处罚决定前,书面告知当事人拟作出处罚决定的事实、理由、依据、处罚内容,以及当事人享有的陈述权、申辩权或听证权。
|
稽查一大队
|
|
决定
|
5.决定责任:依法作出决定;制作《行政处罚决定书》,载明违法事实和证据、处罚依据和内容、申请行政复议或提起行政诉讼的途径和期限等内容。
|
稽查一大队
|
|
送达
|
6.送达责任:行政处罚决定书应当在宣告后当场交付当事人;当事人不在场的,行政机关应当在七日内依照民事诉讼法的有关规定,将行政处罚决定书送达当事人。
|
稽查一大队
|
|
执行
|
7.执行责任:监督当事人在决定的期限内履行生效的行政处罚决定;当事人在法定期限内没有申请行政复议或提起行政诉讼,又不履行的,可依法采取强制措施或申请人民法院强制执行。
|
稽查一大队
|
|
|
8.其他法律法规规章文件规定应履行的责任。
|
稽查一大队
|
|
流程图
|
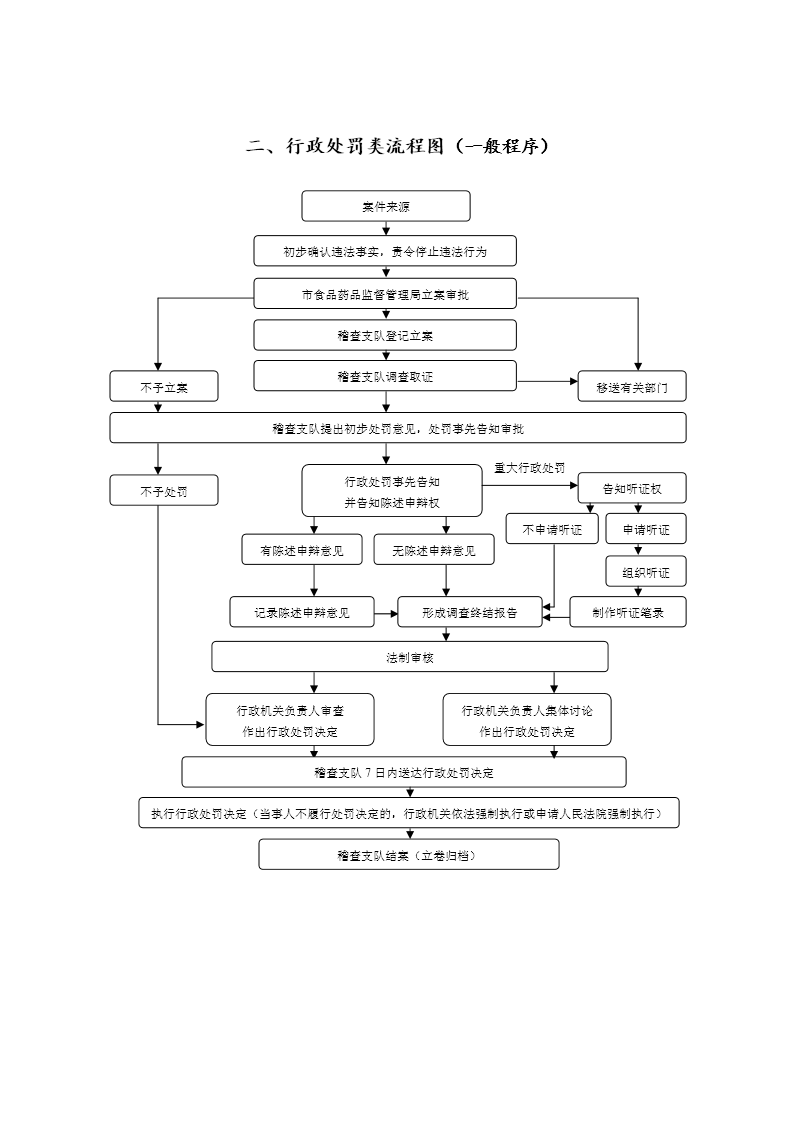
|